[공공투데이 서울=강문정 기자] 길리어드 사이언스 미국 제약사가 개발한 렘데시비르 사용을 미국 식품의약국(FDA)이 정식 승인했다. 22일(현지시간) "항바이러스제인 렘데시비르를 코로나19 입원 환자 치료에 쓸 수 있다는 정식 허가를 내줬다"고 현지 로이터통신과 CNBC방송이 보도 했다.
이에 대해 대니얼 오데이 길리어드 최고경영자(CEO)는 성명을 내고 "코로나19 대유행 시작부터 길리어드는 글로벌 보건 위기의 해법을 찾는 데 도움을 주기 위해 끊임없이 노력했다"며 "1년도 안 돼 미국에서 이 약을 필요로 하는 모든 환자에게 사용 가능하다는 FDA 승인을 얻게 된 것이 믿기지 않는다"고 말했다.
길리어드는 렘데시비르 수요가 급증할 것으로 보고 생산량을 늘리는 데 전력을 기울일 것으로 보인다. 지난 8월 회사 측은 연말까지 200만명 투여분 이상을 생산하고, 내년에 수백만회분을 추가로 더 만들어낼 계획이라고 전했다. 이에 따라 길리어드는 이달 말까지 렘데시비르 생산량이 글로벌 수요를 맞출 수 있을 것으로 기대했다.
원래 렘데시비르는 에볼라 치료제로 사용됐던 정맥주사 형태의 약이다. 코로나19 입원 환자들을 대상으로 한 임상시험에서 효과를 보이며 코로나19 치료제로 주목받았다.
앞서 FDA는 지난 5월 코로나19 치료를 위해 렘데시비르 긴급 사용을 승인한 바 있다. 다만 당시 승인에는 코로나19 팬데믹 기간에만 이 약물을 사용한다는 전제가 깔렸었다. 즉 중증 입원환자들만을 대상으로 다른 약품과 함께 보조치료제 형태로만 사용돼 왔다. 사실상 의사 판단에 처방 가능한 약물이였다.
하지만 최근 세계보건기구(WHO)에서 "렘데시비르가 코로나19 치료에 별다른 도움이 되지 못한다"는 혹평을 받았다. WHO는 연구 결과에서는 렘데시비르가 환자의 입원 기간을 줄이거나 사망률을 낮추지 못한 것으로 나타나 치료 효과를 둘러싼 논란이 지속돼 왔다. 거기다 경증환자에 대해서는 특별한 효과가 입증되지 못했다는 지적도 있었다.
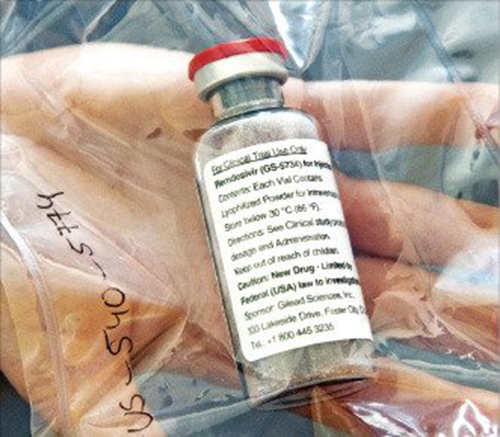
이날 미국 제약사 길리어드 사이언스가 개발한 렘데시비르는 미국에서 코로나19 치료용으로 승인받은 '최초'이자 '유일한' 의약품이 됐다. 코로나19 팬데믹이 시작된 이후 길리어드는 글로벌 보건위기 해법을 찾는데 도움이 되기 위해 쉼 없이 노력해 왔다고 개발 배경을 설명했다.
앞서 지난 3일 도널드 트럼프 미국 대통령도 코로나19에 감염되자 렘데시비르 처방을 받고 입원한지 사흘만에 퇴원했다. 5일 오후 자신의 트위터를 통해 “코로나19를 두려워하지 말라. 이것이 당신의 삶을 지배하도록 하지 말라”는 글을 올렸다. 퇴원후 곧바로 선거 행보를 이어가며 렘데시비르 처방을 받고 완치 했다. 완치한 사유에 대해 렘데시비르 치료제로 인해 완치됐는지는 확인 되지 않았다.
결국 다음달 3일 미국 대선을 코앞에 둔 트럼프 대통령이 다급해 지자 '자신의 선거에 유리한 판세를 끌기위해 코로나19 치료제로 '렘데시비르 FDA 승인 카드'를 쓴 것이 아니냐"는 분석이 나오고 있다.
앞서 길리어드는 지난 8월 회사 측은 연말까지 200만명 투여분 이상을 생산하고, 내년에 수백만회분을 추가로 더 만들어낼 계획이라고 말해, 이후 글로벌 수요을 맞추기 위한 전력을 가할 것으로 보인다.
국내에서도 지난 6월3일 렘데시비르가 특례수입을 승인해 다음달인 7월 1일 국내에 공급됐다. 같은 달 24일에는 정식 품목 허가를 받았다. 질병관리청에 따르면 이달 13일 기준 렘데시비르는 병원 62곳에서 코로나19 환자 600명에게 투여됐다.
렘데시비르 부작용 사례가 국내에서도 나타났다. 이달 국회 보건복지위원회 정춘숙 의원(더불어민주당)이 식품의약품안전처에서 받은 '렘데시비르 부작용 보고 현황'에 따르면 올해 9월 말을 기준으로 보고된 부작용은 총 11건 이었다. 간 기능 수치 상승 3건을 비롯해 발진 3건, 심실 주기의 수축·두드러기가 각 2건, 구토 1건 등이었다.
렘데시비르 가격은 미국의 경우 치료비가 상당히 비싸다. 1바이알(병)당 390달러(약 46만원)로 5일 치료시 2340달러(277만원), 10일 치료 시 4290달러(509만원)이다. 다만 우리나라에서는 아직까지 환자 본인에게 부담 시키지는 않고 있다.
한편 이날 길리어드 주가는 FDA 승인 발표날 시간외 거래에서 2.28달러(3.76%) 급등한 62.95달러에 거래됐다.
/강문정 기자
공공투데이는 인터넷신문위원회 윤리강령을 준수합니다
'당신의 눈과 귀가 뉴스가 됩니다'
"당신의 제보가 사회를 변화 시킬수 있습니다"
공공투데이는 당신의 소중한 제보를 기다립니다.
☎ 제보: [기사제보] 여기 클릭 !!

